Абстрактный
Внутриопухолевые адаптации с появлением резистентных клонов после иммунотерапии, направленной на Т-клетки, представляют собой серьезное препятствие для достижения длительных ремиссий при множественной миеломе. В результате комплексного геномного, транскриптомного и эпигеномного исследования клональных плазматических клеток мы наблюдали антигенный дрейф в 68,4% случаев рецидива после терапии с использованием Т-клеточного активатора GPRC5D (TCE) ( n = 21). Эти события ускользания были обусловлены тремя различными мутационными механизмами, включающими: (1) очаговые и крупные биаллельные делеции в локусе гена GPRC5D ; (2) моноаллельную делецию в сочетании с однонуклеотидными вариантами GPRC5D или вставками/делециями (инделами) на оставшемся аллеле; а также (3) эпигенетическое подавление промотора/энхансера GPRC5D . Помимо биаллельных делеций, приводящих к полной потере антигена, мы демонстрируем, что однонуклеотидные варианты и инсерции/делеции GPRC5D мутируют эпитопы связывания анти-GPRC5D TCE или, чаще всего, затрагивают консервативные мотивы семейства G-белковых рецепторов, критически важные для транспорта белков через мембрану, что приводит к захвату GPRC5D эндоплазматическим ретикулумом. В отдельных случаях совместно возникали множественные субклоны, несущие различные геномные изменения в локусе GPRC5D , что указывает на их конвергентные эволюционные траектории. Следует отметить, что анти-GPRC5D TCE с различной специфичностью, аффинностью и валентностью по-разному воздействовали на мутантные субклоны, подчеркивая их недублирующие функциональные роли в преодолении резистентности.
Похожий контент просматривают другие пользователи.
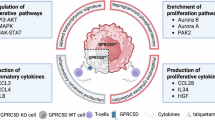
Потеря GPRC5D усиливает пролиферативную способность и конкурентоспособность миеломы при иммунотерапии антителами к GPRC5D.
Источник: www.nature.com