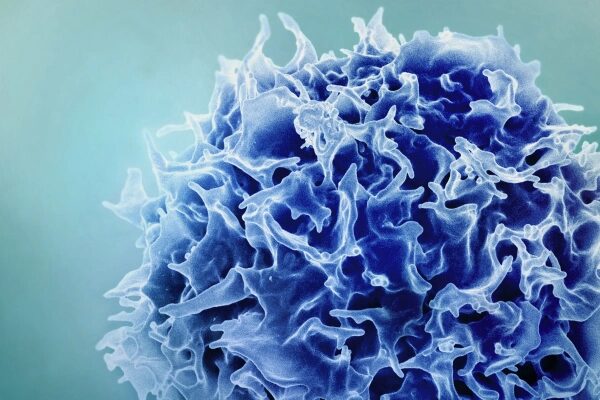
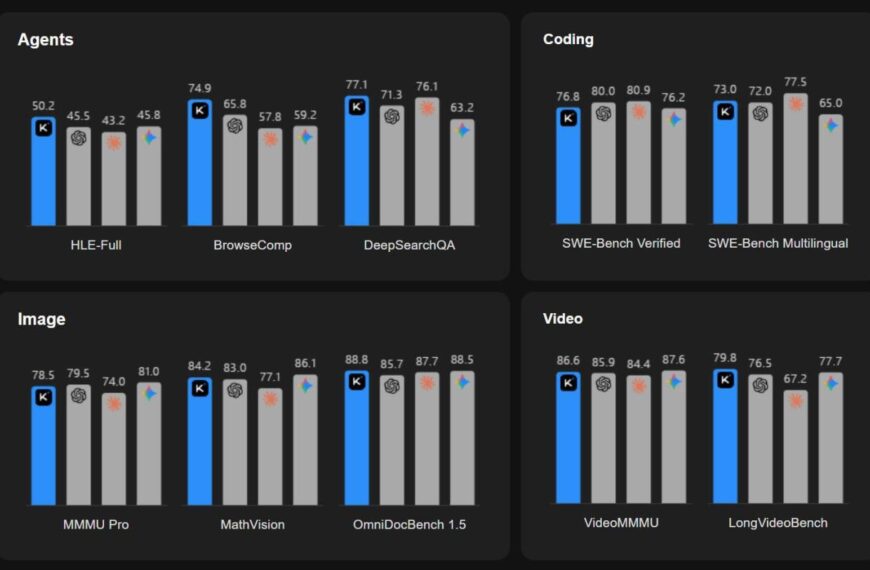
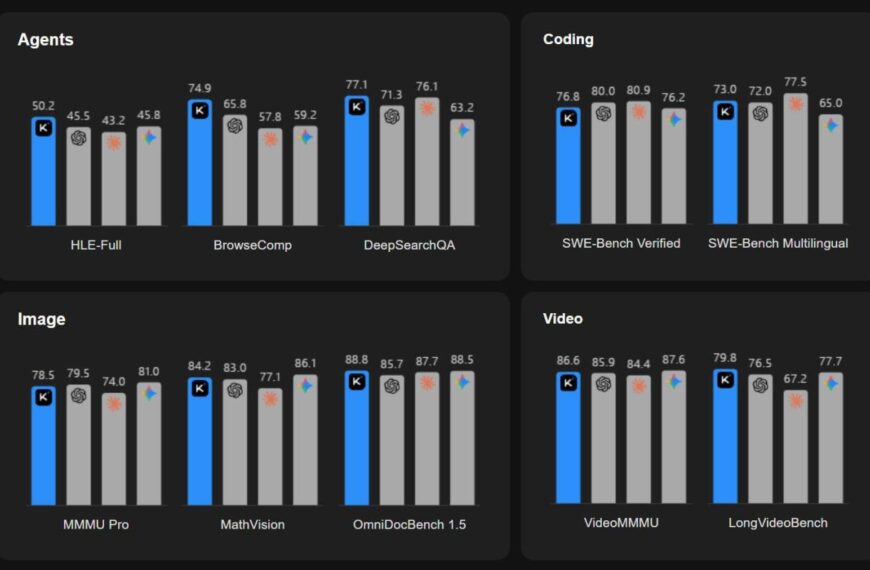
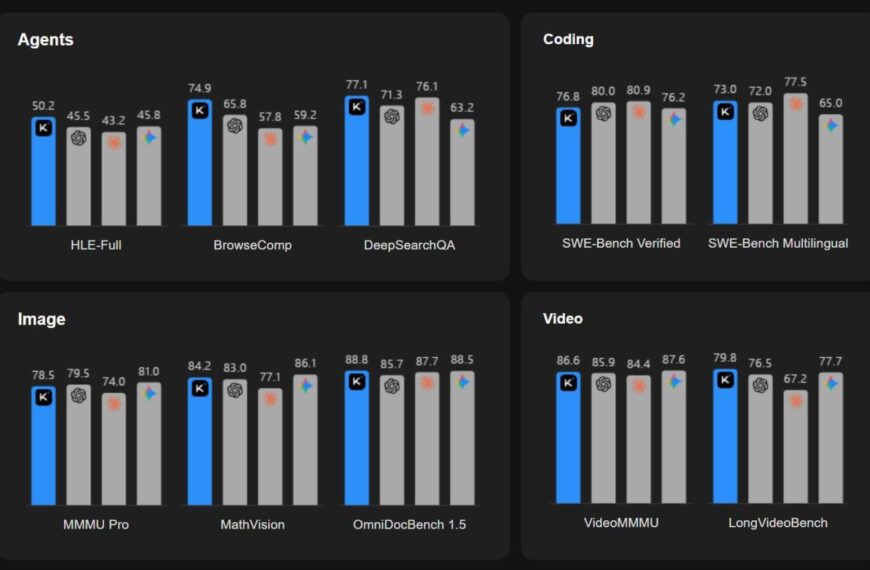
«Зонтичный» CRISPR: выход из тупика регулирования и экономики
Когда двенадцать лет появилась технология генного редактирования CRISPR, ее называли «величайшим биотехнологическим прорывом века», но реальность оказалась куда прозаичнее: один одобренный препарат, около 40 пациентов и ощущение, что индустрия упёрлась в потолок.
История стартапа Aurora Therapeutics, привлёкшего $16 млн от Menlo Ventures и заручившегося поддержкой Дженнифер Дудны, наглядно показывает, где именно застрял CRISPR. Проблема не в том, что мы не умеем редактировать гены — мы умеем это слишком хорошо. Проблема в том, что классическая модель клинических испытаний и одобрений не масштабируется на реальный генетический ландшафт, где одно заболевание может иметь сотни и тысячи мутаций.
Фенилкетонурия (PKU) — почти идеальный пример этого. Теоретически это «лёгкая цель» для генного редактирования: известен ген, понятен орган-мишень (печень), есть убедительные данные на животных. Практически же — это около 1 600 разных мутаций, и разработка отдельного препарата под каждую из них невозможна ни научно, ни экономически. Поэтому идея Aurora — не «персонализированная терапия» в радикальном смысле, а платформенный компромисс: один почти неизменный ген-редактор, где меняются десятки нуклеотидов из тысяч, чтобы перенацелить его на другую мутацию. 99% препарата остаётся тем же, меняется лишь «настройка».
Это выглядит как сугубо техническая деталь, но на самом деле — попытка переформатировать саму логику регулирования. Не случайно глава FDA Мартин Макари публично заговорил о новом пути для «кастомизированных терапий». Регуляторы постепенно признают: если подход не изменится, CRISPR так и останется технологией для единичных показаний вроде серповидноклеточной анемии — счастливых исключений, где одна мутация подходит всем.
Параллельно развивается и противоположный полюс — ультра-персонализированное редактирование «под одного ребёнка», как в случае младенца KJ Малдуна, где лечение стоило миллионы и и которое нельзя повторить. Это не только научный триумф, но и фармацевтический тупик. Именно между этими крайностями — массовой правкой, «одной для всех», и штучной терапией для одного пациента — сейчас формируется реальное будущее генного редактирования.
Кризис CRISPR сегодня — не научный, а институциональный. Технология опережает правила игры. Если «зонтичные» клинические программы заработают, CRISPR может наконец выйти за пределы десятков пациентов и начать лечить тысячи — пусть и не всех. Это конечно не та утопическая революция, которую обещали в 2010-х, но это взрослая, индустриальная версия генного редактирования, способная реально изменить клиническую практику.
CRISPR не потерял свой «mojo». Он просто столкнулся с тем, что лечить ДНК оказалось проще, чем переписать регуляции, создать экономику и оправдать ожидания общества.