Новое исследование показывает, что ключ лежит не в производстве молекулы восстановления, а в контролируемом разрушении этой молекулы. Открытие может вдохновить будущую регенеративную медицину.
 Аксолотли в лаборатории профессора Джеймса Монагана. Фотография: Алисса Стоун/Северо-Восточный университет
Аксолотли в лаборатории профессора Джеймса Монагана. Фотография: Алисса Стоун/Северо-Восточный университетСохранить Сохранить
Аксолотль кажется чем-то из научной фантастики. Эта вечно молодая на вид мексиканская саламандра обладает суперспособностью, которая бросает вызов биологии, какой мы ее знаем: способностью регенерировать целые конечности, части своего сердца и даже спинной мозг. Но как ампутированная конечность узнает, регенерировать ли целую руку от плеча вниз или только кисть от запястья? Эта тайна «позиционной идентичности» очаровывала ученых на протяжении десятилетий.
Команда Северо-Восточного университета под руководством Джеймса Монагана раскрыла ключевой фрагмент этой биологической головоломки. В исследовании, опубликованном в Nature Communications, исследователи раскрывают элегантный молекулярный механизм, который действует как система координат GPS для регенерации клеток. Удивительно, но секрет заключается не в том, чтобы производить больше химического сигнала, а в том, как быстро он разрушается.
В лаборатории Монагана содержится около 500 аксолотлей, о которых заботится команда, состоящая из студентов-бакалавров и постдокторантов. «Выращивание аксолотлей подразумевает управление сложной водной системой и терпение, поскольку они достигают половой зрелости в течение года. Это медленнее, чем с другими модельными организмами, но и более захватывающе. Во многих экспериментах команда исследует совершенно новую территорию», — говорит Монаган.
Более двух десятилетий лаборатория Монагана изучает аксолотля, чтобы понять, как он регенерирует сложные органы, такие как конечности, спинной мозг, сердце и хвост. Исследования его лаборатории сосредоточены на раскрытии того, почему нервы необходимы для этого процесса и какие уникальные клеточные свойства позволяют аксолотлям регенерировать ткани, которые не могут другие животные. Эти открытия могут изменить наше понимание регенерации тела и иметь важное применение в регенеративной медицине.
«В течение многих лет мы знали, что ретиноевая кислота, производное витамина А, является важнейшей молекулой, которая кричит клеткам: «Постройте плечо!»», — объясняет Монаган. «Но загадка заключалась в том, как клетки в регенерирующей культе конечности контролировали свои уровни так точно, чтобы точно знать, где они находятся на оси от плеча до руки».
Чтобы разгадать эту тайну, команда сосредоточилась на кластере стволовых клеток, которые образуются в месте раны после потери конечности у животных, таких как аксолотль, которые способны к регенерации. Известная как бластема, именно эта основа стволовых клеток затем управляет регенерацией. Преобладающая теория состояла в том, что различия в выработке ретиноевой кислоты могут объяснить, почему ампутация плеча (проксимальная) приводит к регенерации всей конечности, в то время как ампутация запястья (дистальная) регенерирует только руку.
«Нашим большим сюрпризом стало открытие того, что ключ был не в том, сколько ретиноевой кислоты было произведено, а в том, как она расщеплялась», — говорит Монаган. Команда обнаружила, что клетки в дистальной части конечности, запястье, переполнены ферментом CYP26B1, единственной функцией которого является разрушение ретиноевой кислоты. Напротив, клетки плеча практически не имеют этого фермента, что позволяет ретиноевой кислоте накапливаться до высоких уровней.
Эта разница создает химический градиент вдоль конечности: много ретиноевой кислоты в плече, мало в запястье. Именно этот градиент информирует клетки об их точном местоположении.
У людей этот путь клеточной пластичности отсутствует или закрыт. «Поэтому главная задача — понять, как вызвать это бластематическое состояние в наших клетках, ключевую переходную структуру в регенерации. Если это будет достигнуто, наши клетки смогут снова реагировать на позиционные и регенеративные сигналы, как это происходит у аксолотля», — объясняет исследователь.
Обманывая клетки, заставляя их чрезмерно регенерировать
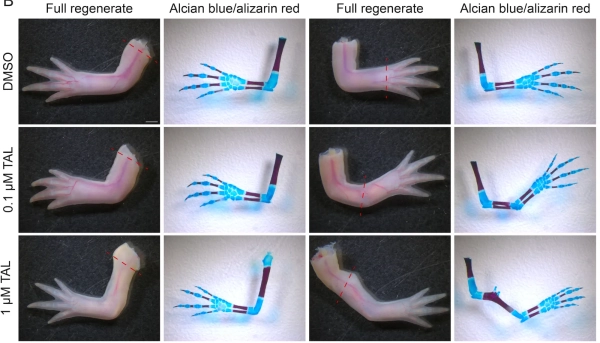
Чтобы подтвердить свое открытие, исследователи провели эксперимент. Они ампутировали ноги аксолотля у запястья и ввели препарат под названием таларозол, который ингибирует фермент CYP26B1. «Отключая тормоза», ретиноевая кислота накапливалась до чрезвычайно высоких уровней в месте, где ее обычно не должно было быть. В результате клетки запястья, «сбитые с толку» высокой концентрацией ретиноевой кислоты, интерпретировали положение как плечо. Вместо того чтобы регенерировать руку, они приступили к регенерации полной, дублированной конечности. «Это был окончательный тест», — говорит Монаган.
Различные регенерации конечностей аксолотлей, обработанных таларозолом.
Фотография: Алисса Стоун/Северо-Восточный университетКоманда пошла еще дальше, чтобы определить, какие гены активируются этими высокими уровнями ретиноевой кислоты. Они обнаружили главный ген, который активировался конкретно в области плеч: Shox. Аббревиатура от «гена гомеобокса низкого роста», Shox так называется потому, что мутации в нем у людей вызывают низкий рост. «Мы определили Shox как важнейшее руководство по эксплуатации в этом процессе», — объясняет Монаган. «Это ген, который сообщает развивающимся клеткам «строить кости руки и предплечья»».
Чтобы подтвердить это, команда использовала технологию редактирования генов Crispr, чтобы вырубить ген Shox у эмбрионов аксолотля. Полученные животные имели необычные конечности: руки и пальцы нормального размера, но значительно более короткие и недоразвитые руки и предплечья. Это показало, что Shox необходим для формирования проксимальных, но не дистальных структур, показывая, что регенерация использует различные генетические программы для каждого сегмента конечности.
Это исследование не только решает давнюю загадку регенеративной биологии, но и предоставляет молекулярную дорожную карту. Понимая, как аксолотль считывает и выполняет свои генетические инструкции для регенерации, ученые могут начать думать о том, как когда-нибудь мы научимся писать свои собственные генетические инструкции.
«Аксолотль обладает клеточными свойствами, которые мы хотим понять на самом глубоком уровне», — говорит Монаган. «Хотя регенерация полной человеческой конечности все еще остается областью научной фантастики, каждый раз, когда мы обнаруживаем часть этого генетического проекта, например, роль CYP26B1 и Shox, мы становимся на шаг ближе к пониманию того, как организовать сложное восстановление тканей у людей».
Чтобы приблизить эту науку к клиническим приложениям, одним из важнейших шагов является успешное индуцирование бластематических образований стволовых клеток в местах ампутации у людей. «Это «святой Грааль» регенеративной биологии. Понимание минимальных компонентов, из которых она состоит — молекулярных сигналов, клеточной среды, физиологических условий — позволило бы нам преобразовать шрам в регенеративную ткань», — объясняет Монаган.
В его текущих исследованиях все еще есть пробелы, которые необходимо заполнить: как регулируется градиент CYP26B1, как ретиноевая кислота связывается с геном Shox и какие последующие факторы определяют формирование определенных структур, таких как плечевая или лучевая кости.
От исцеления к регенерации
Монаган объясняет, что аксолотли не обладают «волшебным геном» регенерации, но имеют те же фундаментальные гены, что и люди. «Главное отличие заключается в доступности этих генов. В то время как травма у людей активирует гены, которые вызывают рубцевание, у саламандр происходит дедифференциация клеток: клетки возвращаются в эмбриональное состояние, в котором они могут реагировать на сигналы, такие как ретиноевая кислота. Эта способность возвращаться в «состояние развития» является основой их регенерации», — объясняет исследователь.
Итак, если у людей те же гены, почему мы не можем регенерировать? «Разница в том, что саламандра может повторно получить доступ к этой [программе развития] после травмы». Люди не могут — они получают доступ к этому пути развития только во время начального роста до рождения. «Мы испытывали селективное давление, чтобы закрыться и исцелиться», — говорит Монаган. «Моя мечта и мечта сообщества — понять, как осуществить переход от рубца к бластеме».
Монаган говорит, что в теории не было бы необходимости модифицировать человеческую ДНК, чтобы вызвать регенерацию, а нужно было бы вмешаться в нужное время и в нужном месте в организме с помощью регуляторных молекул. Например, молекулярные пути, которые сигнализируют клетке о том, что она должна быть расположена в локте со стороны мизинца, а не большого пальца, можно было бы реактивировать в регенеративной среде с помощью таких технологий, как Crispr. «Это понимание можно было бы применить в терапии стволовыми клетками. В настоящее время выращенные в лаборатории стволовые клетки не знают, «где они находятся», когда их трансплантируют. Если их можно запрограммировать с помощью точных позиционных сигналов, они могли бы правильно интегрироваться в поврежденные ткани и способствовать структурной регенерации, например, формированию полноценной плечевой кости», — говорит исследователь.
После многих лет работы понимание роли ретиноевой кислоты, изучаемой с 1981 года, является источником глубокого удовлетворения для Монагана. Ученый представляет себе будущее, в котором заплатка, наложенная на рану, может реактивировать программы развития в клетках человека, имитируя регенеративный механизм саламандры. Хотя это и не произойдет немедленно, он считает, что клеточная инженерия для индукции регенерации — это цель, уже достижимая для науки.
Он размышляет о том, как аксолотль обрел вторую научную жизнь. «Это была доминирующая модель сто лет назад, затем она вышла из употребления на десятилетия, а теперь снова появилась благодаря современным инструментам, таким как редактирование генов и анализ клеток. Команда может изучать любой ген и клетку в процессе регенерации. Кроме того, аксолотль стал культурным символом нежности и редкости».
Источник: www.wired.com