Большое депрессивное расстройство (БДР) — это серьёзная глобальная проблема здравоохранения и одна из ведущих причин инвалидности. Примерно у 30% людей с диагнозом депрессия развивается резистентная к лечению депрессия (РТД), то есть их симптомы недостаточно улучшаются при применении стандартных антидепрессантов. Кетамин привлёк внимание как быстродействующий антидепрессант для людей с РТД. Однако учёные до конца не понимают, как он работает в человеческом мозге, что затрудняет усовершенствование и персонализацию этого лечения.
Новое исследование, опубликованное в журнале Molecular Psychiatry 5 марта 2026 года, попыталось прояснить эту загадку. Исследование возглавил профессор Такуя Такахаши с кафедры физиологии Высшей медицинской школы Университета города Йокогама в Японии. Команда использовала передовой метод позитронно-эмиссионной томографии (ПЭТ) для непосредственного наблюдения за изменениями в рецепторе α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты глутамата (AMPAR). Этот рецептор является ключевым белком, регулирующим связь между клетками головного мозга и играющим важную роль в синаптической пластичности и глутаматергической сигнализации у пациентов, получающих кетамин.
Профессор Такахаши пояснил: «Хотя кетамин продемонстрировал быстрый антидепрессивный эффект у пациентов с резистентной к лечению депрессией, его молекулярный механизм действия в головном мозге человека остается неясным».
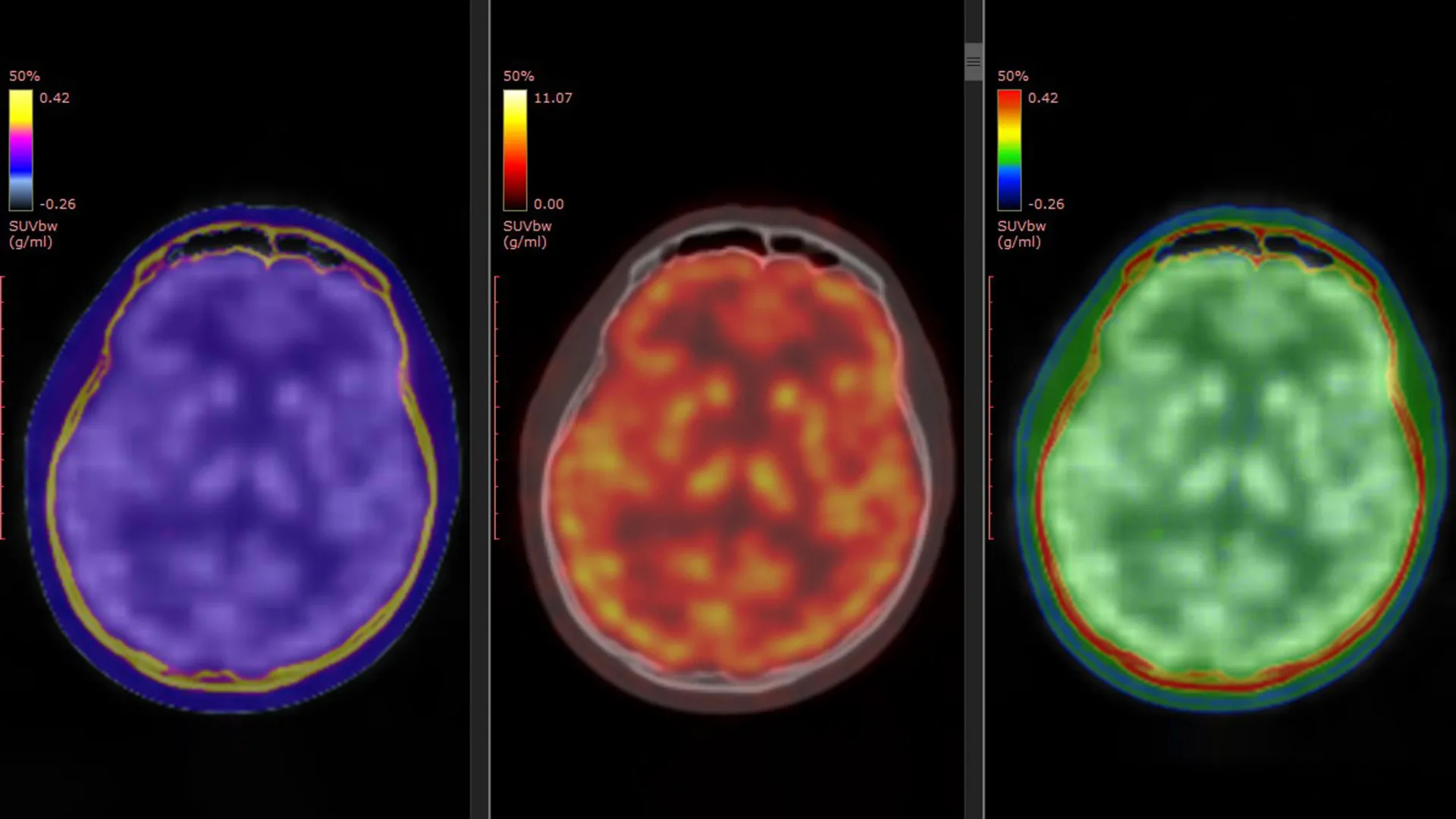
Визуализация рецепторов головного мозга с помощью нового ПЭТ-трассера.
В исследовании использовался разработанный ранее командой ПЭТ-трассер, известный как [¹¹C]K-2. Этот трассер позволяет ученым визуализировать AMPAR на поверхности клеток непосредственно в живом человеческом мозге. Предыдущие лабораторные и экспериментальные исследования на животных показали, что антидепрессивное действие кетамина связано с активностью AMPAR. Новое исследование предоставляет первые прямые доказательства того, что этот процесс происходит у человека.
Для проведения исследования ученые объединили данные трех зарегистрированных клинических испытаний, проведенных в Японии. В группу исследования вошли 34 пациента с диагнозом резистентной к лечению депрессии и 49 здоровых участников, которые служили контрольной группой.
Пациенты получали внутривенно кетамин или плацебо в течение двух недель. ПЭТ-сканирование головного мозга проводилось до начала лечения и повторно после последней инфузии. Такой подход позволил исследователям сравнить изменения уровней и распределения AMPAR в головном мозге с течением времени.
Регионально-специфические изменения в головном мозге связаны с облегчением симптомов.
Результаты показали, что у людей с резистентной к лечению депрессией наблюдались широко распространенные отклонения в плотности AMPAR по сравнению со здоровыми участниками исследования. Эти различия проявлялись в отдельных областях мозга, а не в мозге в целом.
Кетамин не вызывал равномерных изменений по всему мозгу. Вместо этого улучшение симптомов депрессии было связано с динамическими, регионально-специфическими изменениями уровня AMPAR. В некоторых областях коры головного мозга наблюдалось увеличение плотности рецепторов, в то время как в областях, связанных с обработкой вознаграждения, особенно в хабенуле, отмечалось их снижение. Эти регионально-специфические сдвиги были тесно связаны с улучшением симптомов депрессии у пациентов.
«Антидепрессивный эффект кетамина у пациентов с резистентной к лечению депрессией опосредован динамическими изменениями AMPAR в живом человеческом мозге», — пояснил профессор Такахаши. «Используя новый ПЭТ-трассер [11C]K-2, мы смогли визуализировать, как кетамин изменяет распределение AMPAR в определенных областях мозга и как эти изменения коррелируют с улучшением симптомов депрессии».
Эти наблюдения предоставляют прямые доказательства на людях, подтверждающие механизмы, ранее выявленные в исследованиях на животных, и связывающие их с реальным клиническим антидепрессивным эффектом.
Потенциальный биомаркер для прогнозирования эффективности лечения
Полученные результаты не только проясняют механизм действия кетамина, но и могут иметь практическое клиническое значение. ПЭТ-визуализация AMPAR потенциально может служить биомаркером, помогающим врачам оценивать и прогнозировать реакцию пациентов с резистентной к лечению депрессией на лечение кетамином.
Поскольку многие пациенты не реагируют на стандартные антидепрессанты, выявление надежных биологических маркеров эффективности лечения остается важной задачей в психиатрической помощи.
На пути к более персонализированным методам лечения депрессии
Благодаря возможности непосредственного наблюдения за активностью AMPAR в живом человеческом мозге, это исследование помогает преодолеть давний разрыв между лабораторными исследованиями и клинической психиатрией. Результаты показывают, что модуляция AMPAR является центральным механизмом, лежащим в основе быстрого антидепрессивного эффекта кетамина, и предполагают, что ПЭТ-визуализация AMPAR может в будущем способствовать разработке более персонализированных стратегий лечения.
В конечном итоге, эта работа может способствовать разработке более точных методов лечения для людей, страдающих от резистентной к терапии депрессии.
Данная работа была поддержана Министерством образования, культуры, спорта, науки и технологий (Специальные координационные фонды содействия развитию науки и технологий); Японским агентством медицинских исследований и разработок (AMED) (номера грантов: JP18dm0207023, JP19dm0207072, JP24wm0625304, JP25gm7010019 и JP20dm0107124); Японским обществом содействия науке KAKENHI (номера грантов: 22H03001, 20H00549, 20H05922, 23K10432, 19H03587, 20K20603, 22K15793 и 21K07508); Научным фондом Такеда; Программой исследовательских проектов следующего поколения Кэйо; Медицинским исследовательским фондом SENSHIN. а также Японского фонда исследований в области клинической фармакологии.
Источник: www.sciencedaily.com