Если вы когда-либо проходили ПЭТ, вы знаете, какое это испытание. Сканирование помогает врачам выявлять рак и отслеживать его распространение, но сама процедура — настоящий логистический кошмар для пациентов.
Всё начинается с голодания в течение четырёх-шести часов перед госпитализацией. И вам повезло, если вы живёте в сельской местности, и в вашей местной больнице нет ПЭТ-сканера. По прибытии в больницу вам вводят радиоактивный материал, после чего нужно ждать час, пока он выведется из организма. Затем вы входите в ПЭТ-сканер и должны попытаться лежать неподвижно в течение 30 минут, пока рентгенологи делают снимок. После этого вам необходимо физически дистанцироваться от пожилых людей, молодёжи и беременных женщин в течение 12 часов, потому что вы буквально полурадиоактивны.
Ещё одно узкое место? ПЭТ-сканеры сосредоточены в крупных городах, поскольку их радиоактивные индикаторы должны производиться на близлежащих циклотронах — компактных ядерных установках — и использоваться в течение нескольких часов, что ограничивает доступ в сельские и региональные больницы.
Но что, если бы можно было использовать ИИ для преобразования изображений КТ, которые гораздо более доступны и экономичны, в изображения ПЭТ? Именно об этом говорит идея RADiCAIT, оксфордского спин-оффа, который в этом месяце вышел из тени, получив 1,7 миллиона долларов предварительного финансирования. Бостонский стартап, вошедший в двадцатку финалистов Startup Battlefield на конференции TechCrunch Disrupt 2025, только что открыл сбор средств на 5 миллионов долларов для продвижения своих клинических испытаний.
«Что мы на самом деле сделали, так это взяли самое ограниченное, сложное и дорогостоящее решение для медицинской визуализации в радиологии и заменили его самым доступным, простым и недорогим решением — КТ», — рассказал TechCrunch Шон Уолш, генеральный директор RADiCAIT.
Секрет успеха RADiCAIT заключается в его базовой модели — генеративной глубокой нейронной сети, изобретенной в 2021 году в Оксфордском университете командой под руководством соучредителя стартапа и главного специалиста по медицинской информации Регента Ли.
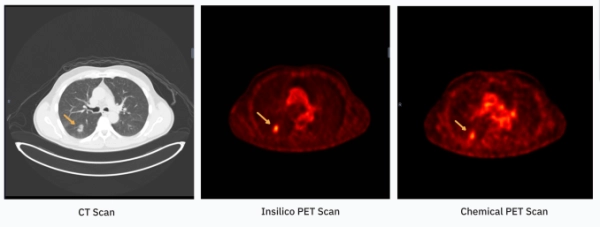
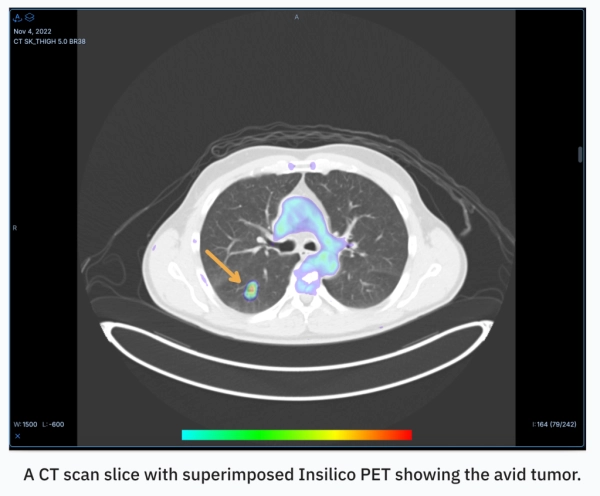
Модель обучается, сравнивая КТ- и ПЭТ-снимки, картируя их и выявляя закономерности в их взаимосвязи. Сина Шаханде, главный технолог RADiCAIT, описывает это как установление связи между «отдельными физическими явлениями» путём перевода анатомической структуры в физиологическую функцию. Затем модель обращается к тому, чтобы уделять особое внимание конкретным особенностям или аспектам сканов, например, определённым типам тканей или аномалиям. Это целенаправленное обучение повторяется многократно на множестве различных примеров, чтобы модель могла определить, какие закономерности имеют клиническое значение.
Финальное изображение, которое отправляется на рассмотрение врачам, создаётся путём объединения нескольких моделей, работающих вместе. Шахандех сравнивает этот подход с AlphaFold от Google DeepMind, ИИ, совершившим революцию в прогнозировании структуры белков: обе системы учатся переводить один тип биологической информации в другой.
Уолш утверждает, что команда RADiCAIT может математически доказать, что их синтетические или сгенерированные ПЭТ-изображения статистически подобны реальным химическим ПЭТ-сканам.
«Именно это показывают наши испытания, — сказал он, — что качество решений было одинаковым, когда врач, рентгенолог или онколог получал химическую ПЭТ или [нашу ПЭТ, созданную с помощью ИИ]».
RADiCAIT не обещает заменить необходимость ПЭТ-сканирования в определённых терапевтических ситуациях, например, при радиолигандной терапии, которая уничтожает раковые клетки. Однако для диагностики, стадирования и мониторинга технология RADiCAIT может сделать ПЭТ-сканирование устаревшим.

«Поскольку система настолько ограничена, предложения недостаточно для удовлетворения спроса на диагностику и тераностику», — сказал Уолш, имея в виду медицинский подход, сочетающий диагностическую визуализацию (например, ПЭТ) с таргетной терапией для лечения заболеваний (например, рака). «Поэтому мы стремимся удовлетворить этот спрос в области диагностики. Сами ПЭТ-сканеры должны компенсировать нехватку в области тераностики».
RADiCAIT уже начал клинические пилотные проекты, специально предназначенные для тестирования на рак лёгких, совместно с такими крупными системами здравоохранения, как Mass General Brigham и UCSF Health. Сейчас стартап проводит клинические испытания в FDA — более дорогостоящий и сложный процесс, который и является основой посевного раунда финансирования RADiCAIT в размере 5 миллионов долларов. После одобрения проекта следующим шагом станет проведение коммерческих пилотных проектов и демонстрация коммерческой жизнеспособности продукта. RADiCAIT также планирует запустить тот же процесс — клинические пилотные проекты, клинические испытания, коммерческие пилотные проекты — для лечения колоректальных заболеваний и лимфомы.
Шахандех отметил, что подход RADiCAIT к использованию ИИ для получения достоверных данных без бремени сложных и дорогостоящих тестов «широко применим».
«Мы изучаем возможности расширения нашей области радиологии», — добавил Шахандех. «Мы ожидаем увидеть аналогичные инновации, связывающие области материаловедения с биологией, химией и физикой, где можно изучать скрытые взаимосвязи природы».
Если вы хотите узнать больше о RADiCAIT, присоединяйтесь к нам на конференции Disrupt, которая пройдёт с 27 по 29 октября в Сан-Франциско. Узнайте больше здесь.

Источник: techcrunch.com