Всё больше исследований свидетельствует о том, что клеточный метаболизм — химические реакции, обеспечивающие энергию и строительные материалы, — играет жизненно важную, но часто недооцениваемую роль на первых этапах жизни. Комментарий Сохранить статью Прочитать позже

Эмбрион плодовой мухи растет, а затем образует слои специализированных клеток. Новые исследования показывают, как метаболизм влияет на эти ранние этапы развития.
Введение
Каждый из нас начинает жизнь как одна клетка. Чтобы развиться в сложное многоклеточное существо, эта клетка должна делиться, а затем эти клетки должны делиться снова и снова — и затем эти стволовые клетки начинают специализироваться на различные типы, с разной судьбой в нашем организме. В первую неделю наши клетки достигают своей первой поворотной точки: они должны стать либо плацентой, либо эмбрионом. Затем, в развивающемся эмбрионе, клетки образуют три основных слоя — эктодерму, мезодерму и эндодерму — которые со временем становятся кожей, нейронами, сердцем, кишечником и так далее.
Эти определения судьбы клеток — в какой тип специализированных клеток они превратятся — происходят поэтапно на протяжении всего эмбрионального развития. Поскольку каждый тип клеток имеет характерный паттерн генной активности, ученые предположили, что решения, принимаемые клетками, диктуются генами: а именно, сетями генов, которые включают и выключают друг друга, запуская каскад, который формирует правильные типы клеток в правильном порядке.
Но гены — это еще не вся история. Новые исследования показали, насколько важен, но недооцененный роль клеточного метаболизма — химических реакций внутри клетки, обеспечивающих энергию и материалы для роста, — в определении судьбы клетки.
«Метаболизм в стволовых клетках, особенно в эмбриональных, — это не просто поддержание жизнедеятельности», — говорит Ян Жилич, биолог-эмбриолог из Копенгагенского университета. «Это важнейший механизм, регулирующий процессы принятия решений».
В ходе своей бурной биохимической активности клетки не только производят энергию, но и синтезируют метаболиты: молекулярные биологические строительные блоки, такие как аминокислоты, нуклеотиды, углеводы и липиды. В последние одно-два десятилетия, с развитием более совершенных методов измерения метаболитов в клетках, значительно возрос интерес к различным способам, которыми эти небольшие молекулы регулируют активность генов, и в частности, судьбу и развитие клеток. Теперь исследования показывают, что их присутствие или отсутствие — на которое могут влиять внешние факторы, такие как окружающая среда и диета — может определять судьбу клетки и, в свою очередь, развитие эмбриона.

Специалист по биологии развития Ян Жилич наблюдал, как один-единственный тип метаболита может изменить судьбу клетки на самых ранних стадиях развития человека.
«Помимо биоэнергетики, эти побочные продукты метаболизма используются также для регулирования специализированных программ», таких как дифференциация клеток и формирование трех слоев эмбриона, — говорит Берна Созен, биолог-эмбриолог из Йельского университета, недавно опубликовавшая в журнале Nature исследование, показывающее, как метаболизм глюкозы влияет на самые ранние стадии эмбрионального развития. «Возможности просто захватывающие. Это действительно меняет наше представление о биологии развития, о том, как начинается наша собственная жизнь».
Традиционно ученые считали, что все инструкции, необходимые клетке для превращения в определенный тип, закодированы в ее ДНК. В этом случае, когда стволовая клетка дифференцируется, часть этого процесса включает в себя активацию генов, кодирующих метаболизм этого типа клетки, — говорит Джаред Раттер, биохимик из Университета Юты. Но исследования теперь показывают, что этот процесс может протекать в обратном направлении: клетка проверяет, есть ли у нее необходимые материалы в окружающей среде. Если она не может осуществить метаболизм, то она не станет этим типом клетки, несмотря на сигналы к дифференциации. «Это революция в моем понимании того, как метаболизм влияет на процессы», — сказал Раттер.
Данная работа опровергает предположения о чистом доминировании генов в процессе развития и помогает нам понять факторы, которые способствуют выживанию эмбриона, гибели клеток и даже развитию рака.
«Практически любой вопрос находится на рассмотрении», — сказала Лидия Финли, биолог-онколог из Мемориального онкологического центра Слоан-Кеттеринг в Нью-Йорке. «Область метаболизма и развития сейчас действительно активно развивается, и это невероятно захватывающе, потому что это еще очень ранняя стадия».

Лидия Финли из онкологического центра Memorial Sloan Kettering обнаружила, что противоопухолевый белок p53 помогает предотвратить рак, регулируя метаболическое состояние клетки.
Ранние сигналы
Один из самых ярких примеров того, как метаболизм может влиять на дифференциацию клеток, можно найти у скромного слизевика. Когда Dictyostelium получает достаточно питательных веществ, он успешно растёт и делится группами отдельных клеток. Но когда пища заканчивается, происходит изменение: отдельные клетки объединяются и образуют своего рода многоклеточного слизня, который ползает как единое целое и формирует плодовые тела для размножения. Хотя доступность пищи является очевидным триггером этого изменения, до недавнего времени никто точно не знал, как именно происходит переключение с одноклеточности на многоклеточность — своего рода определение судьбы клетки — на молекулярном уровне.
Четыре года назад иммунолог Эрика Пирс и ее команда, изучающая клеточный метаболизм в Университете Джонса Хопкинса, обнаружили, как этот переключатель запускается метаболическим путем. В условиях голодания митохондрии Dictyostelium генерируют выброс активных форм кислорода — небольших, нестабильных молекул, которые могут повреждать белки и ДНК, а также выступать в качестве сигнальных молекул. Для защиты от собственных митохондрий клетка вырабатывает антиоксидант под названием глутатион.
Глутатион не появляется из ниоткуда: для его образования необходима сера. Голодающая клетка слизевика направляет всю свою серу на производство глутатиона. Это означает, что серы не остается для построения железо-серных комплексов, без которых клетка не может создавать новые митохондрии. Поэтому у слизевика «нет иного выбора, кроме как стать многоклеточным», — сказал Пирс. Он больше не может расти и распространяться самостоятельно, поэтому превращается в слизня и отправляется на поиски пищи.
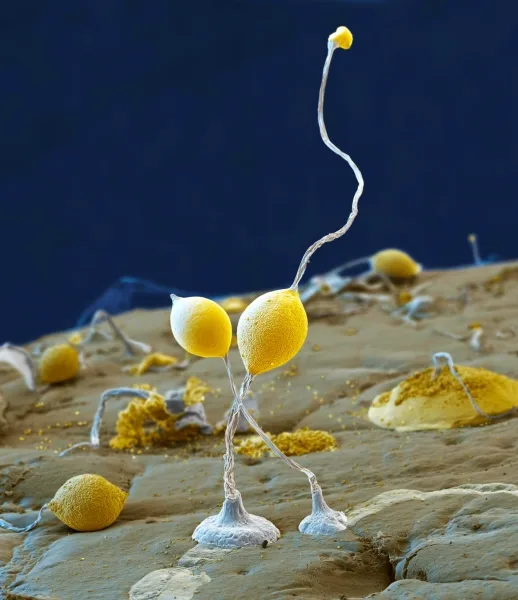
При нехватке пищи слизевик Dictyostelium отказывается от одноклеточного образа жизни и переходит в слизеподобную многоклеточную форму с плодовыми телами (изображение приведено здесь). На клеточном уровне это изменение обусловлено недостатком одного питательного вещества: серы.
«Метаболизм определял весь этот фенотип, и наличие или отсутствие пищи, вероятно, по-прежнему является самой фундаментальной движущей силой», — сказал Пирс. «Каждая наша клетка, вероятно, также подвержена этому воздействию».
Это открытие показало, что метаболическое состояние клетки может запускать каскад сигналов, который полностью изменяет форму и поведение организма. Однако понимание того, как клеточный метаболизм преобразуется в сигнал развития у организмов, более сложных, чем слизистые грибы, потребовало десятилетий работы.
В 1990-х годах биолог Навдип Чандел, будучи аспирантом, изучал митохондриальный фермент, называемый цитохром-с-оксидазой. «Я был довольно самоуверенным молодым человеком, думая, что знаю, что делает цитохром-с-оксидаза: она забирает электрон у цитохрома с и передает его кислороду», — сказал он. — «Это ключевой компонент митохондриального процесса создания клеточной энергии в виде аденозинтрифосфата (АТФ)». Но, к удивлению, в 1996 году исследователи обнаружили, что если цитохром с высвобождается из митохондрий, это запускает каскад сигналов, которые вызывают гибель клеток — своего рода решение о судьбе клетки.
«Таким образом, у цитохрома с есть вторая функция, можно сказать, дополнительная функция», — сказал Чандел. Это был первый намек на то, что митохондрии делают больше, чем просто обеспечивают АТФ: они также влияют на принятие клеточных решений. Чандел, ныне митохондриальный биолог в Медицинской школе Файнберга Северо-Западного университета, с тех пор работает над изучением митохондриальной сигнализации.
Более десяти лет назад, работая с человеческими стволовыми клетками, он обнаружил, что мутация критически важного митохондриального фермента препятствует дифференцировке клеток в жировые клетки, как это должно было бы происходить. В 2013 году его лаборатория показала, что активные формы кислорода, генерируемые митохондриями, являются важными сигналами в развитии кожи у мышей. Затем, в 2023 году, в эксперименте, опубликованном в журнале Nature, он и его команда снова обнаружили, что специализация клеток невозможна без здоровых, функционирующих митохондрий. В мышиной модели стволовые клетки с дефектными митохондриями запускали стрессовую реакцию — каскад молекулярных сигналов, которые активировали гены стрессового ответа в ядре, — после чего клетки останавливались, не в силах стать клетками легких. Легкие мышей не развивались, и они умирали.

Навдип Чандел, биолог из Северо-Западного университета, посвятил свою карьеру изучению того, как митохондриальные сигналы влияют на специализацию клеток и развитие животных.
Чандел пришел к выводу, что стрессовая реакция представляет собой экстренный сигнал ядру о необходимости остановить развитие, когда митохондрии сталкиваются с метаболической проблемой.
«Когда мы начинали эти эксперименты, большинство людей говорили: „Боже мой, какой глупый эксперимент, вы получите мертвые клетки“, — сказал он. — Но подождите. Мы этого не наблюдали. Мы наблюдали специфические дефекты — дефекты в виде недифференцированных клеток. Я думаю, это довольно круто».
В последние несколько лет другие исследовательские проекты независимо друг от друга связали экстренную стрессовую реакцию митохондрий с неспособностью клеток к дифференциации. Например, у плодовых мушек дефекты метаболических ферментов в определенной группе тканей могут вызывать стрессовую реакцию, которая останавливает рост и развитие всего организма. Генетически блокируя стрессовую реакцию, исследователи обратили этот эффект вспять.
Совсем недавно, в феврале 2025 года, в журнале Science эндокринолог Скотт Солейманпур из Мичиганского университета обнаружил, что у мышей с дефектными митохондриями бета-клетки (особые клетки, вырабатывающие инсулин) дедифференцируются — теряют свою идентичность бета-клеток и возвращаются к более незрелому состоянию. Подавляя стрессовую реакцию, его команда смогла заставить бета-клетки редифференцироваться, подобно тому как Чандел смог восстановить клетки легких у своих мышей, подавив их стрессовую реакцию.
Исследователям уже было известно, что митохондрии, находящиеся в состоянии стресса, могут посылать сигналы другим частям клетки. Эти исследования помогают уточнить этот сигнал. «Животное знает, что на метаболическом уровне что-то не так, и оно посылает сигналы, чтобы замедлить развитие», — сказал генетик Джейсон Теннессен из Университета Индианы, возглавлявший исследования плодовых мушек.
Исследование изменило представление Теннессена о взаимосвязи генетики и метаболизма. «Вместо того чтобы думать о том, что сети экспрессии генов просто взаимодействуют с метаболизмом, на самом деле именно метаболизм управляет [принятием решений в процессе развития]», — сказал он, — «а сети экспрессии генов — это инструменты, с помощью которых это происходит».
Идея о том, что клеточный метаболизм является неотъемлемой, но недооцененной частью процесса развития, не является фантастической. В другой области биологии, эпигенетике, исследователи уже подробно описали процесс, посредством которого метаболиты включают и выключают гены. Но им понадобилась работа биологов, изучающих развитие, чтобы связать воедино больше фактов.
Метаболическое ядро
Практически все типы клеток в вашем организме — клетки печени, клетки сердца, клетки кожи, бета-клетки и так далее — содержат один и тот же геном в своих ядрах. Различие заключается в способе регуляции активности генов. В каждом типе клеток экспрессируется разный набор генов, необходимых для синтеза белков и РНК, которые позволяют им правильно функционировать в соответствии со своими функциями в зрелом организме.
За последние несколько десятилетий эпигенетики, изучающие этот процесс, расшифровали сложную систему, с помощью которой белки и ферменты активируют или подавляют определенные гены. В каждой клетке многометровая нить ДНК намотана вокруг белков, называемых гистонами. С помощью специфических ферментов молекулы, которые ученые называют «химическими модификациями» или «эпигенетическими метками», прикрепляются к гистонам и вызывают разматывание ДНК, обнажая различные гены для активации. Таким образом, эти модификации могут активировать одни гены и деактивировать другие, влияя на биохимические процессы в клетке и, следовательно, на функции, которые эта клетка выполняет.
«Эти химические модификации, которые украшают [гистоны] и изменяют экспрессию генов, — это метаболиты, и точка», — сказал Финли, биолог, специализирующийся на изучении рака. «Сами химические модификации являются метаболитами, и их удаление зависит от метаболитов».
Пятнадцать лет назад, когда Кэтрин Веллен работала постдоком, изучая раковые клетки, она обнаружила, что эпигенетические метки на гистонах изменяются в ответ на наличие питательных веществ. Когда пищи много, митохондрии производят метаболит, называемый ацетил-КоА. Он проникает в ядро, где находится геном, через большие поры. Там ферменты расщепляют метаболиты на эпигенетические метки, известные как ацетильные группы, и размещают их на гистонах для активации одного набора генов. Однако, когда клетки голодают, ферменты отщепляют ацетильные группы. Часть этих ацетильных групп превращается обратно в ацетил-КоА и потребляется для получения энергии, в то время как другие перерабатываются для активации другого набора генов.
Очевидно, что в ядре происходит интенсивная метаболическая активность. Веллен задался вопросом, обладает ли ядро собственным уникальным метаболизмом и, следовательно, может ли оно рассматриваться как «метаболический компартмент». Работая с Нейтом Снайдером, биохимиком из Медицинской школы имени Льюиса Каца при Университете Темпл, Веллен и другие исследователи разработали новые методы измерения метаболитов в разных частях клетки и обнаружили, что метаболическая активность в ядре не идентична активности, происходящей в других местах.
«Хотя это может показаться очевидным, на самом деле это было не так», — сказал Веллен. Метаболическая активность ядра была специфична для функций этого компартмента, включая эпигенетическую активность. «В ядре находится множество метаболических ферментов, которые динамически регулируются в ядре», — сказал Веллен, который сейчас возглавляет лабораторию в Университете Пенсильвании. «Мы были очень рады этому открытию».
Идея о ядре как метаболическом компартменте стала основополагающей для понимания того, как метаболизм влияет на эмбриональное развитие. В ранних эмбриональных клетках, по мере принятия решений, определяющих превращение клеток в эктодерму, мезодерму и эндодерму, все эпигенетические метки на гистонах перемещаются. Они могут удаляться, добавляться и перемещаться для активации одних генов и подавления других.
«Интересно то, что всё это связано с массовым накоплением метаболических ферментов в ядре», — говорит Жилич, специалист по биологии развития. Эти ферменты синтезируют молекулы, которые затем активируют другие ферменты, удаляющие эпигенетические метки и создающие новые по мере роста, деления и изменения судьбы клеток.
В этот период клетка перемещает множество ферментов из цитоплазмы и митохондрий в ядро. Таким образом, необходимые для активности генов метаболиты могут производиться локально, в ядре, где они необходимы, — сказал Жилич. «Момент, когда происходит перепрограммирование эпигенома, совпадает с моментом, когда ядро фактически используется в качестве метаболического компартмента».
На ранних стадиях развития человека эмбрион представляет собой клеточный шар. Клетки снаружи образуют плаценту; клетки внутри образуют эмбрион. Главное различие между этими двумя типами клеток заключается в активности метаболических генов. Недавно команда Жилича выявила различия между этими клетками в альфа-кетоглутарате, хорошо изученном метаболите, и показала, что этот метаболит ускоряет дифференциацию стволовых клеток в клетки, которые станут плацентой.
Альфа-кетоглутарат контролирует не только дифференцировку стволовых клеток, но и раковых клеток, как обнаружили несколько лет назад команда Финли и другие группы исследователей. Они изучали белок p53, хорошо известный своими противораковыми свойствами; его ген является наиболее часто мутирующим геном при раке человека. В своем исследовании, опубликованном в журнале Nature, они обнаружили, что p53 вызывает накопление альфа-кетоглутарата; этот альфа-кетоглутарат изменяет судьбу раковых клеток, снижая вероятность образования опухолей. Это было поразительно и неожиданно, поскольку исследователи предполагали, что p53 оказывает противораковое действие, напрямую регулируя активность генов. Он также работает, изменяя метаболизм.
«Это особенно интересно, потому что если изменение метаболизма может существенно изменить судьбу клеток, то существует вероятность того, что этим можно будет манипулировать в терапевтических целях, когда аномальные решения о дифференцировке являются причиной заболевания — как, например, при многих формах рака», — сказал Раттер, который не принимал участия в исследовании.
В некотором смысле, это взаимодействие между метаболизмом и генами очевидно: мы знаем, что на жизнь влияют как гены, так и окружающая среда. Эта новая, захватывающая область исследований показывает на молекулярном уровне, как доступные нашим клеткам материалы влияют на их судьбу и на нашу собственную.
Источник: www.quantamagazine.org