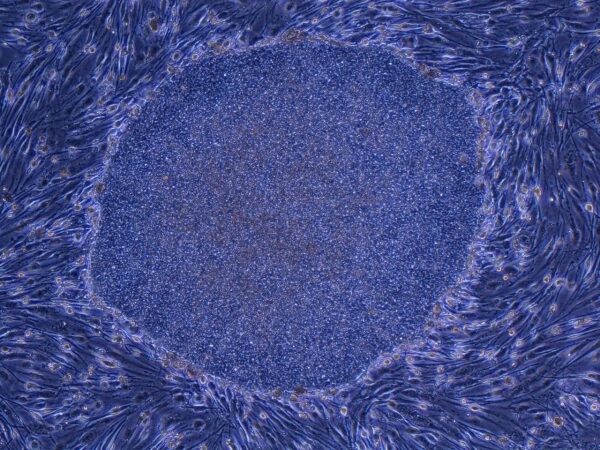
Двадцать лет назад японские исследователи первыми разработали технологию перепрограммирования клеток. Теперь страна впервые выдала разрешение на производство и продажу медицинских изделий, созданных на основе этой технологии. Колония индуцированных плюрипотентных стволовых клеток человека, полученная из фибробластов. Ее фактическая ширина составляет приблизительно 0,5 мм. Фотография: Синья Яманака, Киотский университет. Сохранить эту историю Сохранить эту историю
Колония индуцированных плюрипотентных стволовых клеток человека, полученная из фибробластов. Ее фактическая ширина составляет приблизительно 0,5 мм. Фотография: Синья Яманака, Киотский университет. Сохранить эту историю Сохранить эту историю
6 марта Министерство здравоохранения, труда и социального обеспечения Японии официально выдало условное и ограниченное по времени разрешение на продажу двух регенеративных медицинских препаратов, полученных из перепрограммированных индуцированных плюрипотентных стволовых клеток (iPS-клеток), что совпало ровно с 20-летием создания iPS-клеток у мышей. Это станет первым в мире практическим применением продуктов, полученных из iPS-клеток.
«Мы очень рады, что в 20-ю годовщину объявления о создании индуцированных плюрипотентных стволовых клеток мыши мышей мы сделали важный шаг к их применению в медицине», — сказал Синья Яманака, почетный директор Института исследований индуцированных плюрипотентных стволовых клеток Киотского университета. «Для того чтобы утвердить их в качестве метода лечения, необходимо пройти процесс подтверждения их безопасности и эффективности во многих случаях. Я считаю важным продолжать двигаться вперед неуклонно, шаг за шагом, с научной осторожностью и не поддаваясь соблазну».
Что такое индуцированные плюрипотентные стволовые клетки (iPS-клетки)?
Аббревиатура расшифровывается как индуцированные плюрипотентные стволовые клетки. Это взрослые клетки, такие как клетки кожи или крови, которые были перепрограммированы для функционирования подобно эмбриональным стволовым клеткам. Они могут делиться неограниченно и принимать форму любого типа клеток. Благодаря этой способности их можно использовать для тестирования новых лекарств и для исследований в области регенеративной медицины. Этот тип клеток позволяет продвигать науку без этических проблем, возникающих при работе с эмбриональными стволовыми клетками.
Слои клеток, прикрепленные к стенке сердца.
Одним из одобренных продуктов регенеративной медицины является ReHeart от стартапа Qualipse, базирующегося в Университете Осаки. Это лист специализированных клеток сердца, называемых кардиомиоцитами, дифференцированных из индуцированных плюрипотентных стволовых клеток здоровых доноров, и он вызвал значительный ажиотаж после презентации на выставке Osaka-Kansai Expo. Он предназначен для пациентов с тяжелой сердечной недостаточностью, вызванной ишемической кардиомиопатией, которые не восстанавливаются в достаточной степени, несмотря на стандартное лечение, включая медикаментозную терапию и инвазивные процедуры.
Образец сердечной мышцы, полученный из индуцированных плюрипотентных стволовых клеток (iPS-клеток) компании Qualipse, также привлек к себе большое внимание во время выставки Expo 2005 в Осаке-Кансаи.
Тяжелая сердечная недостаточность — это серьезное состояние, которое со временем ухудшается, и единственными вариантами лечения являются пересадка сердца или искусственное сердце с поддержкой сердца. Однако пересадка сердца затруднена из-за нехватки доноров и возрастных ограничений, а искусственные сердца также несут риск инфекции и повреждения черепных нервов, а также долгосрочное снижение качества жизни.
ReHeart решает эти неудовлетворенные медицинские потребности. Трансплантация проводится хирургическим путем в левой части грудной клетки, при этом три слоя кардиомиоцитов прикрепляются к поверхности сердца. Сигнальные белки, выделяемые трансплантированными клетками, помогают увеличить кровоток и восстановить ткани. В национальном многоцентровом совместном исследовании, в котором участвовали восемь пациентов с тяжелой сердечной недостаточностью, тенденция к улучшению была подтверждена у четырех пациентов: пиковое потребление кислорода (VO2 peak) увеличилось более чем на 10 процентов через 52 недели после трансплантации.
Нейроны «имплантированы» непосредственно в мозг.
Вторым одобренным препаратом является Амусепри (общее название: лагунепроцелл) от компаний Sumitomo Pharma и Racthera. Он представляет собой клетки-предшественники, предназначенные для превращения в нейроны, продуцирующие дофамин, полученные из донорских индуцированных плюрипотентных стволовых клеток. Препарат показан для улучшения двигательных симптомов у пациентов с болезнью Паркинсона, у которых наблюдалась недостаточная эффективность существующих методов медикаментозной терапии, включая препараты, содержащие леводопу.
Болезнь Паркинсона — это нейродегенеративное заболевание, вызывающее двигательные симптомы, такие как тремор конечностей и мышечная ригидность, из-за постепенной потери дофаминергических нервных клеток в головном мозге. Современные лекарственные препараты направлены на облегчение симптомов, а не на фундаментальное восстановление утраченных нервных клеток.
Проект AmShepli предлагает новый вариант лечения путем трансплантации стволовых клеток из утраченных нейронов, вырабатывающих дофамин, непосредственно в мозг. Эта трансплантация проводится с использованием малоинвазивного типа нейрохирургии. В черепе просверливаются небольшие отверстия, по одному с каждой стороны, и клетки распределяются и вводятся в капсулу с обеих сторон тремя путями доставки.
В ходе исследования, проведенного под руководством врачей в больнице Киотского университета, у четырех из шести пациентов с болезнью Паркинсона, участвовавших в исследовании, наблюдалось улучшение показателя «времени выпадения» (показатель, когда действие препарата прекращается) по шкале оценки двигательных симптомов и лечения (MDS-UPDRS, часть III) через 24 месяца после трансплантации. Исследователи подтвердили, что клетки оставались жизнеспособными у всех шести пациентов в месте трансплантации.
Первое в мире производственное предприятие и сотрудничество между промышленностью и научными кругами.
Компания SMaRT, расположенная в городе Суита, префектура Осака, отвечает за производство препарата Amshepri и является первым в мире коммерческим производственным предприятием, специализирующимся на регенеративной медицине и клеточных препаратах, полученных из донорских индуцированных плюрипотентных стволовых клеток (iPS-клеток). iPS-клетки, используемые в качестве сырья для продукта, поступают из запасов, предоставленных Исследовательским фондом iPS-клеток Киотского университета, а технологии индукции дифференцировки и производства основаны на запатентованных технологиях Киотского университета и других учреждений. Например, в части производственного процесса используется технология очистки клеток компании Eisai; создание продукта стало возможным благодаря сотрудничеству между промышленностью и академическими кругами при участии различных учреждений.
Можно также утверждать, что тот факт, что это новаторское одобрение было получено в Японии, был структурно неизбежен. Это объясняется тем, что вся цепочка поставок практически полностью завершена в Японии, начиная с создания базовой технологии Синья Яманакой, лауреатом Нобелевской премии по физиологии или медицине 2012 года, и заканчивая поставкой индуцированных плюрипотентных стволовых клеток (iPS-клеток) Исследовательским фондом iPS-клеток Киотского университета, технологиями индукции дифференцировки и производства, разработанными Киотским университетом и другими учреждениями, созданием коммерческого производственного предприятия SMaRT и даже развитием университетских стартапов и выходом на рынок крупных фармацевтических компаний.
Два новых продукта считаются «одобренными с условиями и сроками». Это означает, что даже после одобрения эффективность и безопасность продуктов должны продолжать подтверждаться посредством пострегистрационных клинических испытаний и исследований конечного применения.
Эта уникальная японская система позволила получить раннее одобрение в таких областях, как регенеративная медицина, где проведение крупномасштабных клинических испытаний затруднено, и является одним из факторов, объясняющих практическое применение этих продуктов. Более того, процесс одобрения, включая долгосрочное государственное финансирование со стороны национальных учреждений, был не только результатом работы отдельных исследователей, но и продуктом японской научной политики.
Эксперимент в открытой лаборатории Института исследований индуцированных плюрипотентных стволовых клеток Киотского университета.
Фотография: Центр исследований и применения индуцированных плюрипотентных стволовых клеток, Киотский университет.Планируется провести всестороннее исследование результатов применения препарата ReHeart у целевого числа 75 пациентов, а начало продаж ожидается примерно осенью 2026 года. Компания AmShepli также обязана собрать данные для официального одобрения.
Это начало регенеративной медицины.
Трансплантация любого из этих продуктов на данном этапе доступна не всем и станет доступна в качестве застрахованного лечения после завершения процедуры страхового покрытия, в ходе которой продукт будет официально зарегистрирован как покрываемый государственной медицинской страховкой. Ориентировочный срок включения этих продуктов в страховой список составляет три месяца после одобрения для фармацевтических препаратов и от четырех до пяти месяцев после подачи заявки на медицинские принадлежности, поэтому ожидается, что пройдет еще некоторое время, прежде чем они дойдут до пациентов.
Комментируя одобрение, министр здравоохранения, труда и социального обеспечения Кеничиро Уэно заявил на пресс-конференции: «Я очень рад, что терапевтический продукт из Японии, созданный на основе индуцированных плюрипотентных стволовых клеток профессора Яманаки, впервые в мире применяется на практике, и я надеюсь, что он поможет пациентам не только в Японии, но и во всем мире».
Джун Такахаши, директор Института исследований индуцированных плюрипотентных стволовых клеток Киотского университета, руководивший испытаниями препарата «Амусепури», заявил: «Результаты обсуждений — это важный шаг вперед, но даже если препарат будет одобрен, это не цель, а лишь начало применения этого нового лекарства». Он подчеркнул важность накопления долгосрочных данных, начиная с осторожного подхода и используя ограниченное количество случаев.
Прошло двадцать лет с момента появления индуцированных плюрипотентных стволовых клеток (iPS-клеток). Технология, зародившаяся в лаборатории, достигла стадии, когда человеческие клетки культивируются, дифференцируются и, наконец, вводятся в организм пациента. Будущее медицины, переписанное iPS-клетками, только начинается.
Источник: www.wired.com